RESUMEN
Objetivo: Evaluar costo-efectividad de la tiroglobulina (TG) como marcador tumoral para la detección de recidivas en pacientes con cáncer diferenciado de tiroides, comparando su desempeño con ultrasonido (USG) y tomografía computarizada (TAC). Métodos: Estudio cuantitativo, descriptivo de evaluación económica en salud, realizado en el Departamento de Oncología del Hospital Militar Escuela Dr. Alejandro Dávila Bolaños entre 2016 y 2020. Se incluyeron 50 pacientes con recurrencia tumoral. Los costos y la efectividad de TG, USG y TAC se analizaron mediante la razón de costo-efectividad incremental (RCEI), con datos recolectados de expedientes clínicos. Resultados: La tiroglobulina tuvo un costo por paciente de $317.14 y una efectividad del 52%. El ultrasonido resultó ser la herramienta más costo-efectiva, con un costo de $204.08 por paciente y una efectividad del 100%. La TAC, aunque igual de efectiva con el 100%, presentó un costo significativamente más alto ($1,031.25 por paciente). La combinación de TG con USG aumentó la sensibilidad diagnóstica, mejorando la detección de recidivas. El análisis RCEI indicó que la TG es menos eficiente y más costosa en comparación con el USG. Conclusión: El ultrasonido debe ser considerado como la herramienta de primera línea para el monitoreo de pacientes con cáncer diferenciado de tiroides, debido a su alta efectividad y menor costo. La tiroglobulina, aunque limitada como único marcador, complementa al USG en estrategias multimodales. Este estudio refuerza la importancia de priorizar herramientas costo-efectivas en la práctica clínica para optimizar el manejo del cáncer de tiroides.
Palabras Clave:
Tiroglobulina, ultrasonido, costo-efectividad, cáncer de tiroides.
ABSTRACT
Objective: To assess the cost-effectiveness of thyroglobulin (TG) as a tumor marker for detecting recurrences in differentiated thyroid cancer (DTC) patients and compare its performance with ultrasound (USG) and computed tomography (CT). Methods: A quantitative, descriptive, and cross-sectional study was conducted in the Oncology Department of the Dr. Alejandro Dávila Bola- ños Military School Hospital from 2016 to 2020. Fifty patients with tumor recurrence were included. Costs and effectiveness of TG, USG, and CT were analyzed using the incremental cost-effectiveness ratio (ICER). Data were collected from clinical records and processed using Excel and SPSS. Results: TG had a cost per patient of $317.14 and an effectiveness of 52%. Ultrasound proved to be the most cost-effective tool, with a cost of $204.08 per patient and an effectiveness of 100%. CT, while equally effective (100%), was significantly more expensive ($1,031.25 per patient). The combination of TG and USG improved diagnostic sensitivity, enhancing recurrence detection. ICER analysis revealed that TG is less efficient and more expensive than USG. Conclusion: Ultrasound should be considered the first-line tool for monitoring patients with DTC recurrences due to its high effectiveness and lower cost. TG, while limited as a standalon marker, complements USG in multimodal strategies. This study underscores the importance of cost-effective diagnostic tools to optimize clinical outcomes and reduce healthcare expenses in oncology management.
Key Words:
Thyroglobulin, ultrasound, cost-effectiveness, thyroid cancer
INTRODUCCIÓN
El cáncer diferenciado de tiroides (CDT) es considerado un problema de salud pública a nivel mundial. Es el 16º cáncer más frecuente, el octavo más frecuente en mujeres y el tumor endocrino más frecuente con el 90%. De los tumores malignos de tiroides, el diferenciado esta entre el 85–90% y el indiferenciado entre el 2–5%1. Para algunos autores, la sobrevida en este tipo de cáncer posee un buen pronóstico, algunos casos han sido reportados 30 años después en monitoreo, aunado a esto fueron pacientes con los subtipos más agresivos y enfermedad más extensa, por ende, se ofreció un seguimiento prolongado una vez realizada la tiroidectomía total (TT) o casi total y en casos seleccionados ablación con I-131 (Yodo)2 .
Los pacientes sometidos a tratamiento y ablación remanente con I-131 pueden generar anticuerpos indetectables de tiroglobulina (AcTg), por lo que el uso de sTg puede ofrecer una alternativa recurrente de tratamiento de la enfermedad2 . Además de esto algunos estudios reportaron su importancia como factor pronóstico, cuando se mide sTg preablativa (pTg) (inmediatamente previo a la administración de I), no ha sido completamente establecido ya que un remanente tiroideo postquirúrgico podría contribuir de forma variable a incrementar su nivel sérico Los pacientes que presentan recurrencia o persistencia de enfermedad tienen valores de pTg más elevados que aquellos que se mantienen libres de enfermedad2,3.
Debido a la incidencia del cáncer de Tiroides que representa el 16% del total de patología oncológica atendidas en el Hospital Militar Escuela Dr. Alejandro Dávila Bolaños (HMEADB), y dado a las diferencias en el seguimiento de los pacientes tiroidectomizados, se persigue con este estudio, aportar resultados útiles que permitan protocolizar este manejo y tener una idea del costo beneficio de la prueba. El análisis de costo-efectividad (ACE) generalmente se define como una evaluación comparativa de dos o más intervenciones en términos de costos y consecuencias. El objetivo de este estudio fue establecer el costo efectividad de la prueba de Tiroglobulina en la detección de recurrencias de los pacientes con carcinoma diferenciado de tiroides del Departamento de Oncología del HMEADB durante el periodo 1 de enero 2016 al 31 de diciembre 2020 y de esta forma fundamentar las directrices que regulen la utilidad de esta en la práctica clínica.
METODOLOGÍA
Se realizó un estudio con enfoque cuantitativo y diseño descriptivo de corte transversal, enfocado en la evaluación económica en salud. La investigación se llevó a cabo en el Departamento de Oncología del HMEADB, ubicado en Managua, Nicaragua. La población estudiada incluyó 768 expedientes clínicos de pacientes de ambos sexos, sometidos a tiroidectomía total y diagnosticados con cáncer diferenciado de tiroides, quienes recibieron seguimiento oncológico durante el período de 2016 a 2020.
La selección de los participantes se basó en criterios predefinidos. Se incluyeron pacientes diagnosticados con carcinoma diferenciado de tiroides que fueron sometidos a tiroidectomía total como tratamiento principal, y evidencia de recidiva tumoral por citología o histopatología; con al menos seis meses de seguimiento médico y expedientes clínicos completos. Se excluyeron aquellos con expedientes incompletos, menos de seis meses de seguimiento o que interrumpieron su atención en el hospital o que no tenían evidencia de recidiva tumoral.
Las variables de estudio abarcaron características sociodemográficas, como edad, sexo, ocupación y origen; características clínicas, como el tipo de carcinoma (bien diferenciado, moderadamente diferenciado o pobremente diferenciado), niveles de tiroglobulina pre y post operatorios, y tiempo de recurrencia tumoral. Además, se evaluaron los costos asociados al uso de tiroglobulina como marcador tumoral, en comparación con métodos alternativos como Ultrasonido (USG), Tomografia Axial Computarizada (TAC) y Resonancia Magnética Nuclear (RMN), así como la efectividad de cada método en la detección de recidivas.
La recolección de datos se basó en fuentes secundarias mediante la consulta de expedientes clínicos del hospital. La información se registró en fichas diseñadas específicamente para el estudio, compuesta por 20 preguntas que incluyeron datos sociodemográficos, clínicos y económicos. Los datos recopilados fueron procesados en Microsoft Excel y SPSS, utilizando análisis estadístico descriptivo para caracterizar la población y análisis de costo-efectividad para comparar los métodos evaluados. La efectividad de cada técnica se calculó con base en la tasa de detección de recidivas, y los costos se analizaron considerando tanto valores unitarios como frecuencia de uso.
Para la comparación entre métodos, se utilizó la Razón de Costo-Efectividad Incremental (RCEI), lo que permitió determinar el costo adicional por unidad de efectividad lograda con el uso de tiroglobulina frente a métodos alternativos. El procesamiento incluyó la aplicación de la fórmula RCEI, considerando los costos y la efectividad de cada alternativa. La fórmula para su obtención es:
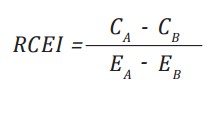
donde CA y EArepresentan el coste y la efectividad de la alternativa objeto de estudio, mientras que CB y EB son los correspondientes a la alternativa estándar de comparación. La efectividad y costos de la tiroglobulina fueron CA y EA y las demás alternativas como ultrasonido, como TAC o RMN fueron C(X) y E(X).
Los sesgos de selección y de medición se minimizaron a partir de los criterios de inclusión y exclusión mencionados anteriormente, conformando así la uniformidad de los datos extraídos de los expedientes clínicos estandarizados, de esta manera la selección se contempló siguiendo las recomendaciones establecidas por Sessler4 y minimizar los errores aleatorios, definiendo las pautas metodológicas y el análisis estadístico a partir del diseño estadístico transversal, previniendo la aleatorización y ajustando la muestra que se completaría con los expedientes revisados, en este sentido como no se emplearon instrumentos de medición adicionales, esto evitó variabilidad en las medidas y controló el sesgo de medición, ya que los expedientes son documentos legales con altos estándares de calidad de los datos y la disponibilidad de la información depende de los valores reales observados según ocurrencia y magnitud. Al utilizar registros médicos contemporáneos, se eliminó el riesgo de sesgos de memoria. Además, un único investigador recolectó los datos, garantizando consistencia y objetividad.
En términos éticos, se obtuvo autorización del hospital para acceder a los expedientes clínicos, garantizando la confidencialidad y privacidad de los datos de los pacientes. La información recolectada fue utilizada exclusivamente con fines de investigación, respetando los principios éticos aplicables a estudios en salud.
RESULTADOS
Entre el 1 de enero de 2015 y el 31 de diciembre de 2020, se registraron 50 pacientes con recurrencia de cáncer diferenciado de tiroides en el Departamento de Oncología del HMEADB. De estos, el 74% (37 pacientes) correspondían a mujeres y el 26% (13 pacientes) a hombres. La distribución por sexo de los pacientes se presenta en la (Tabla 1).
En relación con la edad, la mayor frecuencia de pacientes se concentró en el rango de 31 a 40 años, representando el 30% del total, seguido por el grupo de 21 a 30 años, con un 22%. Estos dos grupos comprenden más de la mitad de los pacientes. En los grupos de mayor edad, se observó una disminución gradual: el 14% correspondía a pacientes entre 41 y 50 años, y el 22% a pacientes de 51 a 60 años. La proporción de pacientes disminuyó drásticamente a partir de los 61 años, con solo el 2% entre 61 y 70 años y un 10% con más de 70 años. El promedio de edad fue de 43.9 años, con un rango de 21 a 75 años. En total, 52% (26) pacientes eran menores de 40 años.
En cuanto a la procedencia, 64% (32) pacientes residían en el área urbana, mientras que 36% (18) provenían del área rural. Esto indica una mayor representación de pacientes urbanos con recurrencia tumoral.
Tabla 1. Características sociodemográficas de los pacientes con recidiva de cáncer diferenciado de Tiroides en el Departamento de oncología del Hospital Militar Escuela Dr. Alejandro Dávila Bolaños 2016 al 2020.
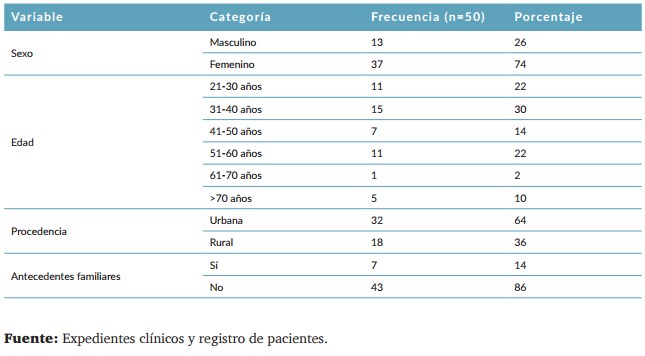
Respecto a los antecedentes familiares de cáncer de tiroides, se encontró que el 86% (43) pacientes no tenían antecedentes, mientras que solo el 14% (7) pacientes reportaron antecedentes familiares de este tipo de cáncer.
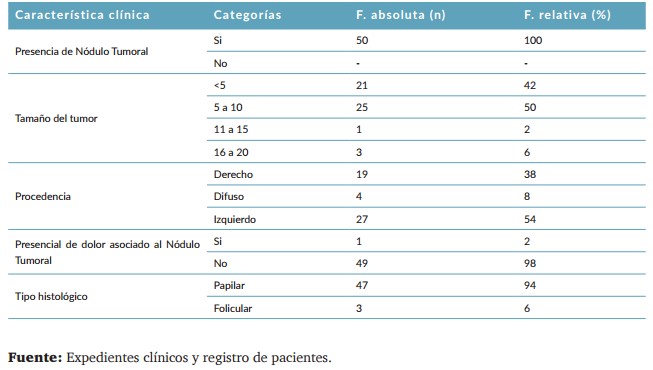
En cuanto a la presencia de nódulos tumorales, todos los pacientes con recidiva, es decir, el 100% (n=50), presentaron nódulos tumorales recidivante, (Tabla 2).
Respecto al tamaño del tumor recidivante, para los pacientes que tuvieron la recidiva, el 50% (25), de los pacientes presentaron nódulos de entre 5 y 10 mm, mientras que el 42% (21) de los pacientes tenían tumores de menos de 5 mm. Solo el 2% (1) paciente tenía un tumor de entre 11 y 15 mm, y 6% (3) pacientes presentaban nódulos con un tamaño de 16 a 20 mm. En relación con la localización del nódulo, 54% (27) pacientes tenían nódulos en el lóbulo izquierdo, mientras que 38% (19) pacientes presentaban nódulos en el lóbulo derecho. Por otro lado, 8% (4) pacientes tenían nódulos con una distribución difusa. Esta caracterización clínica aporta la información adicional para la efectividad en la detección de la recidiva, específicamente para el resultado de la tiroglobulina, ya sea positivo o negativo y el número de pruebas realizadas.
En cuanto a la presencia de dolor asociado al nódulo, solo 2% (1) paciente reportó dolor, mientras que la gran mayoría 98% (49) pacientes no presentaban dolor relacionado con el nódulo tumoral. En lo referente al tipo histológico, el 94% de los pacientes (47) fueron diagnosticados con carcinoma papilar, mientras que el 6% (3) presentaron carcinoma folicular, (Tabla 2).
Tabla 2. Características clínicas de los pacientes con recidiva activa de cáncer diferenciado de Tiroides en el Departamento de oncología del Hospital Militar Escuela Dr. Alejandro Dávila Bolaños 2016 al 2020.
En la (Tabla 3) se aprecia que los 50 pacientes con recurrencia de cáncer de tiroides se realizaron 518 estudios de tiroglobulina entre 49 pacientes para un promedio por paciente de 10.57 (estudios/troides, se gastó en total $15,540 dólares en el diagnóstico de pacientes con recurrencia, para un promedio por paciente de $317.1 dólares por pacientes en los 5 años de seguimiento.
De los 50 pacientes con recurrencias, el 52% (26) pacientes tuvieron TG (detectada por ensayo quimioluminiscencia) mayor de 2ng/dl, que es el valor umbral para considerar la TG como alterada en los pacientes con la tiroidectomía. De estos 26 paciente, el 46% (23) de ellos tuvieron TG menor de 2 ng/dl, un paciente no registró TG. Se determinó como unidad de efectividad, la detección de los verdaderos positivos (prueba sensible) detectando entonces ese 52%; se calculó en términos decimales la efectividad de todas las pruebas, siendo para la TG 0.52 de efectividad. De los 23 pacientes con TG menor de 2, a 5 pacientes no se le realizó Anti-Tg y 6 pacientes presentaron Anti-tg mayor de 80. Por lo que hubo 12/50 pacientes (24%) con Anti-tg menor de 80 y no se elevó TG a pesar de la recurrencia. Si se considera que 12 pacientes con recurrencia no elevaron TG, es notable que se invirtió $3,805.2 dólares sin tener resultado esperado, por lo que se tuvo que usar otros medios diagnósticos.
El uso de la Anti-tiroglobulina como parte del diagnóstico de recurrencia en cáncer de tiroides se solicitó en 38 pacientes, de los cuales 8 se usó una sola vez y 30 pacientes de 2 a más; con un rango de 1-23 veces, con un promedio por paciente de 5.8 estudios. Se realizaron un total de 222 estudios de Anti-tg para un monto de $6,660 dólares. El costo por paciente fue $174 dólares. Si consideramos que en los 38 pacientes se hubiera gastado $1,140 dólares, tendríamos un excedente de $5,520 dólares que no se debieron haber gastados.
Otra prueba realizada para el diagnóstico fue el Ultrasonido (USG) de cuello. Se realizaron 200 ultrasonidos en 49 pacientes con cáncer de tiroides, a un paciente se le realizó TAC de cuello y no USG. El USG se debe realizar a los pacientes con tiroidectomía previa cada 6 meses. El rango fue de 0-7 ultrasonido por pacientes para un promedio de 4 ultrasonido por paciente, en los 5 años de seguimiento.
El costo de inversión en pacientes recurrentes con el uso de ultrasonido de cuello fue de $10,000 dólares con un promedio por paciente de $200 dólares. Considerando que de los 49 pacientes que se usó el ultrasonido de cuello, todos tuvieron datos de recurrencia evidenciado por patología. Podemos decir que fue positivo en 49/49 pacientes realizados, por lo tanto, la efectividad del USG es de 1, que corresponde al 100% de los pacientes detectados correctamente. El gold estándar para confirmar la recurrencia ha sido el USG, ya que es una técnica efectiva para visualizar la glándula tiroides y los ganglios linfáticos cervicales, permitiendo identificar la presencia de nuevos nódulos o agrandamiento de ganglios que podrían indicar recurrencia.
De los 50 pacientes que recurrieron, a 32 pacientes se le realizó TAC. El número de TAC realizado fue de 110 estudios en el total de esos 32 pacientes, para un promedio de 2.2 estudios por paciente recurrente; siendo el rango de 1-11 TAC en alguno de los pacientes, es decir que hubo pacientes a quienes se les realizó 1 TAC y otros a quienes se les realizaron 11 TAC. El costo de la TAC es de 300 dólares, por lo que se invirtió en TAC $33,000 dólares, para un promedio por paciente de $1031.25 dólares.
De los 50 pacientes que recurrieron, a 4 pacientes se le realizó resonancia magnética nuclear (RMN). El número de RMN realizado fue de 5 estudios, con un rango de 0-2 estudios por paciente, para un promedio de 0.1 estudios por paciente recurrente y el número de RMN dentro de los que se les indicaron fue 1.25 estudios por paciente. El costo de la RMN fue de 500 dólares, por lo que se invirtió en RMN $2, 500 dólares, para un promedio por paciente recurrente de 50 USD. Tanto la TAC como la RMN su valor es de 1.00 para efectividad.
Tabla 3. Análisis comparativo de alternativas diagnósticas para detección de recidiva activa de cáncer diferenciado de Tiroides en el Departamento de oncología del Hospital Militar Escuela Dr. Alejandro Dávila Bolaños 2016 al 2020.
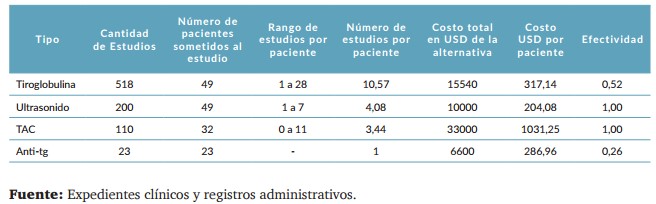
En la figura 1 se aprecia que la tiroglobulina tiene un costo por paciente de $317.14, con una efectividad del 52%. Esto indica que, aunque esta prueba puede ser útil en el seguimiento, su capacidad para detectar recurrencias es relativamente baja. La efectividad de 52% sugiere que menos de la mitad de los casos recurrentes son identificados adecuadamente mediante esta prueba, por lo tanto, podría ser necesario combinar la tiroglobulina con otras pruebas diagnósticas para mejorar la precisión y efectividad del seguimiento.
Con respecto al ultrasonido, se destaca como la opción más favorable, ya que tiene un costo por paciente de $204.08 y una efectividad del 100%. Esto significa que el ultrasonido es altamente efectivo para detectar recurrencias de cáncer de tiroides y, además, es la prueba más económica entre las evaluadas. La combinación de un costo relativamente bajo y una efectividad perfecta sugiere que el ultrasonido debería ser la herramienta de primera línea para el monitoreo de estos pacientes, facilitando así una detección precoz y mejorando los resultados clínicos.
La TAC, aunque tiene una efectividad del 100%, presenta un costo por paciente de $1,031.25, lo que la convierte en una opción significativamente más cara. A pesar de su alta efectividad, el elevado costo plantea dudas sobre su uso rutinario para el seguimiento del cáncer de tiroides, especialmente cuando existen alternativas más económicas e igualmente efectivas como el ultrasonido.
Finalmente, los anticuerpos Anti-tiroglobulina (Anti-tg) tienen un costo de $286.96 y una efectividad de solo 26%. Esta baja efectividad sugiere que esta prueba no es un método confiable para detectar recurrencias, lo que limita su utilidad clínica en el seguimiento de pacientes con cáncer de tiroides.
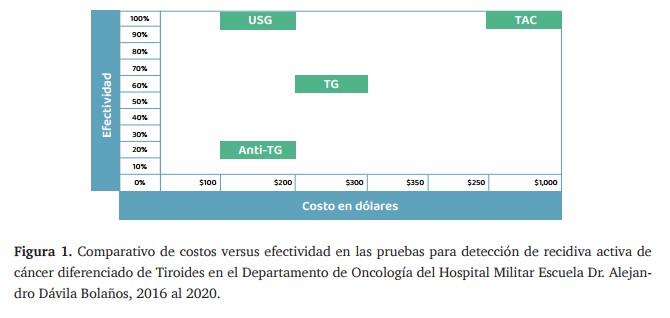
Fuente: Expedientes clínicos y registros administrativos.
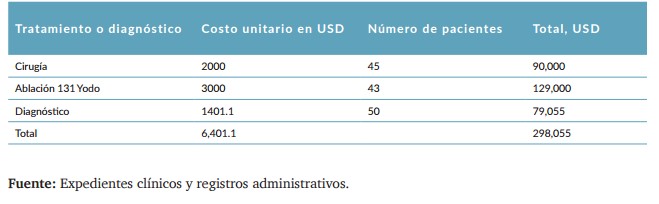
Según el tratamiento realizado a los pacientes (Tabla 4), de los 50 estudiados, a 43 pacientes se les realizó ablación con 131 Yodo, si se considera que el costo del 131 Yodo es de $3000 dólares, el costo total sería de $129,000 dólares para el total de pacientes.
De los pacientes estudiados a 45 pacientes se les realizó cirugía, si consideramos que el costo total de una cirugía de tiroides es de $2000 dólares, el costo total sería de 90,000 dólares. Sumando el diagnóstico más el tratamiento en los 45 pacientes que se les calculó la razón de años de recurrencia/paciente, el costo por paciente es de $6,401 dólares y por cada año/paciente con recidiva el costo es de $2,783 dólares por cada año de vida.
Tabla 4. Costos de tratamiento y diagnóstico unitario y total en pacientes de cáncer diferenciado de Tiroides en pacientes del Departamento de oncología del Hospital Militar Escuela Dr. Alejandro Dávila Bolaños 2016 al 2020.
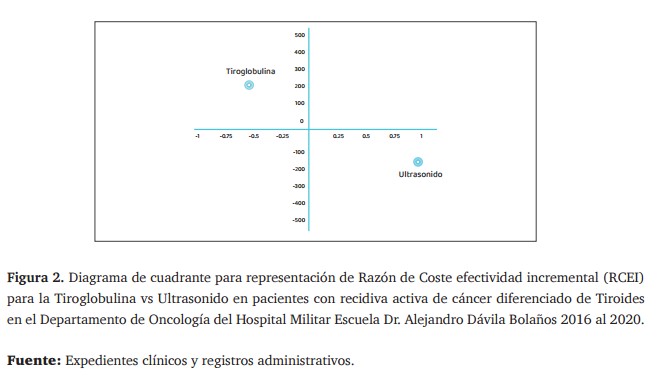
La figura 2 muestra la diferencia entre los costos y efectividad de la TG versus el USG para la detección de recidivas del cáncer de tiroides y para la toma de decisión con respecto al análisis coste-efectividad. Para el primer cuadrante no son recomendables tomar las alternativas, ya que, en comparación al USG la Tiroglobulina es menos efectiva (-0.48) y más cara (113.06 USD) la fórmula utilizada fue:

La diferencia de costos entre la tiroglobulina y el ultrasonido es de 113,06 dólares, lo que indica que el uso de la tiroglobulina implica un costo adicional en comparación con el ultrasonido.
En cuanto a la diferencia en efectividad, se observa un valor de -0,48 al comparar ambas intervenciones. Este valor negativo sugiere que la tiroglobulina es menos efectiva que el ultrasonido en el contexto del análisis realizado, lo que podría implicar que los pacientes que utilizan la tiroglobulina no obtienen un beneficio adicional en términos de resultados de salud en comparación con aquellos que se someten a ultrasonido.
Finalmente, la razón de costo-efectividad incremental (RCEI) se calcula en -235,54. Este valor negativo implica que, por cada unidad adicional de efectividad obtenida al utilizar la tiroglobulina en lugar del ultrasonido, se incurre en un costo negativo, lo que refuerza la conclusión de que la tiroglobulina no solo es menos efectiva, sino que también representa una opción menos favorable desde el punto de vista económico en comparación con el ultrasonido. En general, estos resultados sugieren que, en términos de costo y efectividad, el ultrasonido podría ser una opción más rentable y efectiva que la tiroglobulina para el monitoreo en el contexto analizado.
DISCUSIÓN
El cáncer papilar de tiroides ha mostrado un incremento en el diagnóstico en el HMEADB, lo cual sigue la tendencia observada a nivel mundial5 , donde la incidencia de este tipo de cáncer ha aumentado considerablemente en las últimas décadas, este aumento en los diagnósticos puede atribuirse a varios factores, entre los que destacan el acceso mejorado a pruebas diagnósticas más sensibles y un aumento en la vigilancia médica6 . En este contexto, la planificación de recursos, tanto humanos como financieros, son necesarias para la creciente carga de la enfermedad, en especial cuando se trata de los costos asociados a los pacientes que presentan recurrencia.
Entre los años 2016 y 2020, en el HMEADB se diagnosticaron 50 pacientes con recurrencia, lo que representa una prevalencia del 6.5%. Esta cifra está en línea con la literatura internacional, algunos autores proyectan aumento en el número de diagnósticos y una prevalencia de recidiva del 30%7,8, estas cifras subrayan la importancia de contar con un sistema de seguimiento y control adecuado para estos pacientes, ya que la recurrencia es un evento frecuente en el curso del cáncer de tiroides diferenciado, especialmente en los primeros años tras el tratamiento inicial.
El carcinoma papilar de tiroides fue el tipo histológico más común en nuestra población, lo que concuerda con lo descrito en la literatura internacional, que lo reportan como el subtipo predominante de cáncer de tiroides. García-Torres, describieron una frecuencia de carcinoma papilar en más del 80% de los casos6 , lo que se asemeja a los resultados de nuestro estudio. Este hallazgo es significativo porque el carcinoma papilar suele tener un buen pronóstico, con altas tasas de supervivencia a largo plazo, lo que refuerza la importancia de un seguimiento adecuado para detectar y tratar posibles recurrencias a tiempo.
En cuanto a las características demográficas, tanto el promedio de edad como la distribución por sexo observados en nuestra población se alinean con las referencias internacionales, donde la mayoría de los casos se presentan en mujeres, con un rango de edad que oscila entre los 30 y 60 años9 . Este perfil demográfico es clave para la planificación del seguimiento y tratamiento, ya que permite anticipar necesidades específicas en diferentes grupos de pacientes.
Considerando un paciente en seguimiento, según las National Comprehensive Cancer Network® (NCCN ®) en su versión 3.2024 del año 202410, se deben hacer de 2 a 4 estudios por años, podemos decir de manera general que se hizo buen uso de TG en los pacientes recurrentes con 10.5 estudios por pacientes en período promedio de 5 años.
Un dato muy importante, es que tuvimos 15 pacientes con 4 o más tomografías, de estos 10 pacientes tuvieron más de 15 estudios de tiroglobulina, la característica en común de los pacientes fue la cantidad de consultas multidisciplinarias en donde se repiten estudios en menos de 3 meses. Por lo que se puede tomar medidas administrativas para usar un mismo estudio en diferentes visitas multidisciplinarias.
Se encontró que 12 pacientes de los recurrentes no elevaron Tg, representando el 24 % de falso negativo. Al comparar con la literatura internacional11 se encontró que 25% de pacientes recurrentes pueden no elevar tiroglobulina al inicio de la recurrencia, otro estudio presenta importantes magnitudes de falsos negativos en paciente con recurrencia9 . Consideramos que tuvimos la cantidad de falsos negativos, propios de la enfermedad. Con esto se justifica la combinación con el ultrasonido de cuello para la detección de recurrencias. Esto también refuerza la necesidad de combinar la medición de tiroglobulina con ultrasonido de cuello para mejorar la sensibilidad diagnóstica. En nuestro estudio, el ultrasonido mostró una efectividad del 100%, lo que lo posiciona como una herramienta esencial para la detección de recurrencias, en concordancia con las guías de manejo internacionales.
Al realizar el análisis del tiempo de recurrencia encontramos que el 62.2% de los pacientes que recurrieron fueron en un tiempo menor de 2 años. Esto es esperado ya que la mayoría de las recurrencias en pacientes con cáncer de tiroides se da en los primeros años. Este hallazgo es consistente con estudios previos, como el de Lamartina que indican que la mayoría de las recurrencias en pacientes con cáncer de tiroides diferenciado ocurren durante los primeros dos años de seguimiento12. Esto subraya la importancia de un seguimiento intensivo durante los primeros dos años post-tiroidectomía, cuando el riesgo de recurrencia es mayor. Además, el uso de ultrasonido de cuello durante este periodo crítico podría optimizar la detección precoz y mejorar los resultados clínicos.
El costo del seguimiento en los pacientes con cáncer de tiroides recurrentes fue de $1,401 dólares muy por debajo al costo referido en un estudio publicado por Yang, en 20211 donde ellos refieren $18,829.00 dólares. Si comparamos el costo de años vidas en nuestro estudio fue de $609.1, muy por debajo al costo de año vida reflejado en ese estudio de $1004,22 dólares. Al realizar el costo por paciente que recurre en nuestro estudio, encontramos que por cada paciente que recurre se gasta $6,401 dólares.
Considerando que se tendrán de cada 100 pacientes con cáncer de tiroides, 6 con recurrencia, se debe programar un costo anual adicional al presupuesto en el tratamiento de cáncer de tiroides recurrente de $38,406 dólares, por cada 100 pacientes diagnosticados.
Un elemento sumamente importante es que todos los pacientes con recidiva le fueron encontrados hallazgos positivos en el ultrasonido, sin embargo, es relevante señalar que, debido al diseño del estudio, no fue posible evidenciar el número de falsos positivos que presentaron la alteración y que podrían sobreestimar la efectividad del 100%, por lo que se sugiere la necesidad de estudios que evalúen este hallazgo. Al contrastar los resultados con la literatura, concuerdan con los presentados por Xiangchun Li, donde el ultrasonido de cuello y el uso de tiroglobulina aumentó el diagnóstico de recurrencia a 97.4% de especificidad, 75% de sensibilidad y 93.6% de precisión diagnóstica13, además otros autores reforzaron el uso de ultrasonido como una herramienta diagnostica de uso frecuente en esta etapa14,15.
En nuestro análisis, la tiroglobulina mostró un costo por paciente de $317.14 dólares, con una efectividad del 52%, lo que indica que, a pesar de su utilidad, su capacidad para detectar recurrencias es limitada y ha sido descrito en la literatura16. Este hallazgo es consistente con estudios que reportan un 33.3% de falsos negativos en pacientes con cáncer de tiroides recurrente, lo que sugiere que una proporción significativa de casos puede pasar desapercibida al confiar exclusivamente en este marcador. En contraste, el ultrasonido presentó una efectividad del 100% y un costo de $204.08, destacándose como la herramienta más eficaz y costo-efectiva para el seguimiento de estos pacientes. Si bien algunos autores como Pacini et al.17 resaltan la importancia de utilizar un enfoque multimodal, donde la combinación de tiroglobulina y ultrasonido mejora significativamente la precisión diagnóstica, otros como Cortés et al. la describen como una prueba eficaz para el diagnóstico de recidiva18, sin embargo estudios más recientes sugieren valorar su uso dependiendo de la etapa de la enfermedad así como la vigilancia pre y post operatoria19.
La razón de costo-efectividad incremental (RCEI) entre la tiroglobulina y el ultrasonido proporciona una perspectiva valiosa sobre la eficiencia relativa de estas dos pruebas diagnósticas en el seguimiento de pacientes con cáncer de tiroides. Al calcular la RCEI, se puede observar la relación entre el costo adicional asociado a la tiroglobulina en comparación con el ultrasonido y la diferencia en su efectividad. El RCEI entre la tiroglobulina y el ultrasonido en nuestro estudio fue de -235.5 USD por paciente, esto implica que el uso de tiroglobulina no justifica el costo adicional frente al ultrasonido, que no solo es más económico, sino que también ofrece una efectividad completa.
En el cuadrante para la RCEI (figura.2), demuestra el hecho de que la tiroglobulina haya caído en el primero, indica que es más cara y menos efectiva en comparación con el ultrasonido y tiene implicaciones significativas para su uso en la práctica clínica. Esto indica que siendo más cara y menos efectiva debería de considerarse para su uso, debido a la carga económica que representaría en número de usuarios, de intervenciones y de seguimiento de los pacientes, lo que podría generar una discusión nueva para limitar su uso a casos específicos donde este justificada su utilidad.
CONCLUSIONES
El estudio demostró que el USG es la herramienta diagnóstica costo efectiva con los mejores resultados, además de esto, el costo económico permite identificar que debería ser considerado por encima de la tiroglobulina, que se realizaron con más frecuencia y a menor costo, pero con menor efectividad diagnostica.
En el caso de la Anti-Tiroglobulina, demostró poseer poca eficiencia diagnostica, y se reportaron gastos excesivos diagnósticos con el uso de este método y la TAC, aunque efectiva en el 100% demostró una carga económica alta para el servicio. La limitación en el número de pacientes a quienes se evaluó por resonancia magnética no permitió evaluar la efectividad global. En este contexto, se puede concluir que la tiroglobulina no debería ser considerada como una opción viable para el seguimiento de todos los pacientes con cáncer de tiroides, ya que resulta en un gasto innecesario, sin una mejora en la detección de recurrencias, por lo que su uso debe estar justificado.
REFERENCIAS BIBLIOGRÁFICAS
- Diabetes & Metabolismo AC de E. Resúmenes de las Conferencias Tiroides. Rev Colomb Endocrinol Diabetes Metab [Internet]. 2017 [citado 8 de mayo de 2025];4(2):3. Disponible en:https://shre.ink/xaC1
- Díaz RE, Véliz J, Wohllk N. Importancia de la tiroglobulina sérica preablativa en la predicción de sobrevida libre de enfermedad en cáncer diferenciado de tiroides. Rev Médica Chile [Internet]. diciembre de 2013 [citado 8 de mayo de 2025];141(12):1506-11. Disponible en: https://shre.ink/xaX3
- Fuenzalida-Mery L, González-Arestizábal T, Portilla-Rojas M, Gac-Espinoza P, Rodríguez-Moreno F, Cabané- Toledo P, et al. Análisis de tiroglobulina preablativa y cáncer diferenciado de tiroides preoperatorio. Rev Médica Chile [Internet]. julio de 2022 [citado 8 de mayo de 2025];150(7):855-60. Disponible en: https://shre.ink/xaXr
- Sessler DI, Imrey PB. Clinical Research Methodology 1: Study Designs and Methodologic Sources of Error. Anesth Analg [Internet]. octubre de 2015 [citado 8 de mayo de 2025];121(4):1034-42. Disponible en: https:// journals.lww.com/00000539-201510000-00026
- Domínguez JM, Martínez MT, Massardo JM, Muñoz S, Droppelmann N, González HE, et al. Riesgo de recurrencia en cáncer diferenciado de tiroides: escala MINSAL. Rev Médica Chile [Internet]. marzo de 2018 [citado 8 de mayo de 2025];146(3):282-9. Disponible en: https://www.scielo.cl/scielo.php?script=sci_abstract&pid=S003498872018000300282&lng=es&nrm=iso&tlng=pt
- García-Torres E, Zambrano-Galván G, González JCC. Frecuencia Y Hallazgos Clínicos Del Carcinoma De Tiroides En Pacientes Del Hospital General 450 En La Ciudad De Durango, México. Rev Venez Endocrinol Metab [Internet]. 2021 [citado 8 de mayo de 2025];19(2):97-104. Disponible en: https://www.redalyc.org/ journal/3755/375569374004/html/
- Marcillo-Carvajal C, Rodríguez-Palma GK, Rodríguez-Palma DJ, Zavala-Sánchez VA. Anti-tiroglobulina asociada a la valoración diagnostica del Cáncer de tiroides en Latinoamérica. MQRInvestigar [Internet]. 5 de marzo de 2024 [citado 9 de mayo de 2025];8(1):3716-41. Disponible en: https://www.investigarmqr.com/ojs/ index.php/mqr/article/view/1083
- Hernández A V, Jiménez-López M, Serrano F S, Obregón G G, Pérez M CI, Hernández A V, et al. Factores de riesgo asociados a recidiva de carcinoma papilar de tiroides. Rev Otorrinolaringol Cir Cabeza Cuello [Internet]. marzo de 2019 [citado 9 de mayo de 2025];79(1):67-74. Disponible en: https://shre.ink/xlJb
- Park EK, Chung JK, Lim IH, Park DJ, Lee DS, Lee MC, et al. Recurrent/metastatic thyroid carcinomas false negative for serum thyroglobulin but positive by posttherapy I-131 whole body scans. Eur J Nucl Med Mol Imaging. febrero de 2009;36(2):172-9.
- NCCN Guidelines for Patients: Cáncer de tiroides. 2024.
- Yang N, Yang H, Guo JJ, Hu M, Li S. Cost-Effectiveness Analysis of Ultrasound Screening for Thyroid Cancer in Asymptomatic Adults. Front Public Health. 2021;9:729684.
- Lamartina L, Durante C, Filetti S, Cooper DS. Low-risk differentiated thyroid cancer and radioiodine remnant ablation: a systematic review of the literature. J Clin Endocrinol Metab. mayo de 2015;100(5):1748-61.
- Li X, Zhang S, Zhang Q, Wei X, Pan Y, Zhao J, et al. Diagnosis of thyroid cancer using deep convolutional neural network models applied to sonographic images: a retrospective, multicohort, diagnostic study. Lancet Oncol. febrero de 2019;20(2):193-201.
- McCoy KL, Yim JH, Tublin ME, Burmeister LA, Ogilvie JB, Carty SE. Same-day ultrasound guidance in reoperation for locally recurrent papillary thyroid cancer. Surgery [Internet]. 1 de diciembre de 2007 [citado 9 de mayo de 2025];142(6):965-72. Disponible en: https://www.surgjournal.com/article/ S0039-6060(07)00546-6/abstract
- Franco-Castañeda X, Chala-Galindo AI, Franco-Castañeda X, Chala-Galindo AI. Localización intraoperatoria de las recurrencias en cáncer de tiroides mediante la inyección de azul de metileno guiada por ecografía. Rev Colomb Cir [Internet]. diciembre de 2021 [citado 9 de mayo de 2025];36(4):611-9. Disponible en: http://www.scielo.org.co/scielo.php?script=sci_abstract&pid=S201175822021000400611&lng=en&nrm=iso&tlng=es
- Rico-Morlán FJL, Hernández-Cuéllar A, Martínez-Macías R, Barra-Martínez R, Santiago-Vázquez RY. Niveles séricos de tiroglobulina como marcador de malignidad en pacientes con nódulo tiroideo. Gac Mex Oncol [Internet]. 1 de marzo de 2009 [citado 8 de mayo de 2025];8(2):54-61. Disponible en: http://www.elsevier.es/es-revista-gaceta-mexicana-oncologia-305-articulo-niveles-sericos-tiroglobulina-como-marcador-X166592010950179X
- Pacini F, Sabra MM, Tuttle RM. Clinical relevance of thyroglobulin doubling time in the management of patients with differentiated thyroid cancer. Thyroid Off J Am Thyroid Assoc. julio de 2011;21(7):691-2.
- Cortés J, Escalada J, Ángeles Vicente M, Ignacio Alonso J, Irigoyen L, Maldonado G, et al. La prueba de tiroglobulina tras hormona estimulante de la tiroides recombinante modifica la estrategia del seguimiento del cáncer diferenciado de tiroides. Endocrinol Nutr [Internet]. 1 de noviembre de 2006 [citado 8 de mayo de 2025];53(9):543-9. Disponible en: https://shre.ink/xaVK
- Indrasena BSH. Use of thyroglobulin as a tumour marker. World J Biol Chem [Internet]. 26 de febrero de 2017 [citado 8 de mayo de 2025];8(1):81-5. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/ articles/PMC5329716/
 .
.